近日,汕头大学医学院第二附属医院泌尿外科林浩主任医师团队与中山大学附属第一医院泌尿外科黄斌教授(汕头大学医学院第二附属医院泌尿外科兼聘教授)合作,在肿瘤学领域顶级期刊《Cancer Research》(2023年影响因子12分)上发表了题为“MTHFD2 Enhances cMYC O-GlcNAcylation to Promote Sunitinib Resistance in Renal Cell Carcinoma”的研究论文,揭示了MTHFD2介导舒尼替尼的耐药新机制,为晚期肾癌患者提供精准治疗新策略。附二院林浩主任医师为该论文的共同第一作者,黄斌教授为论文的通讯作者。
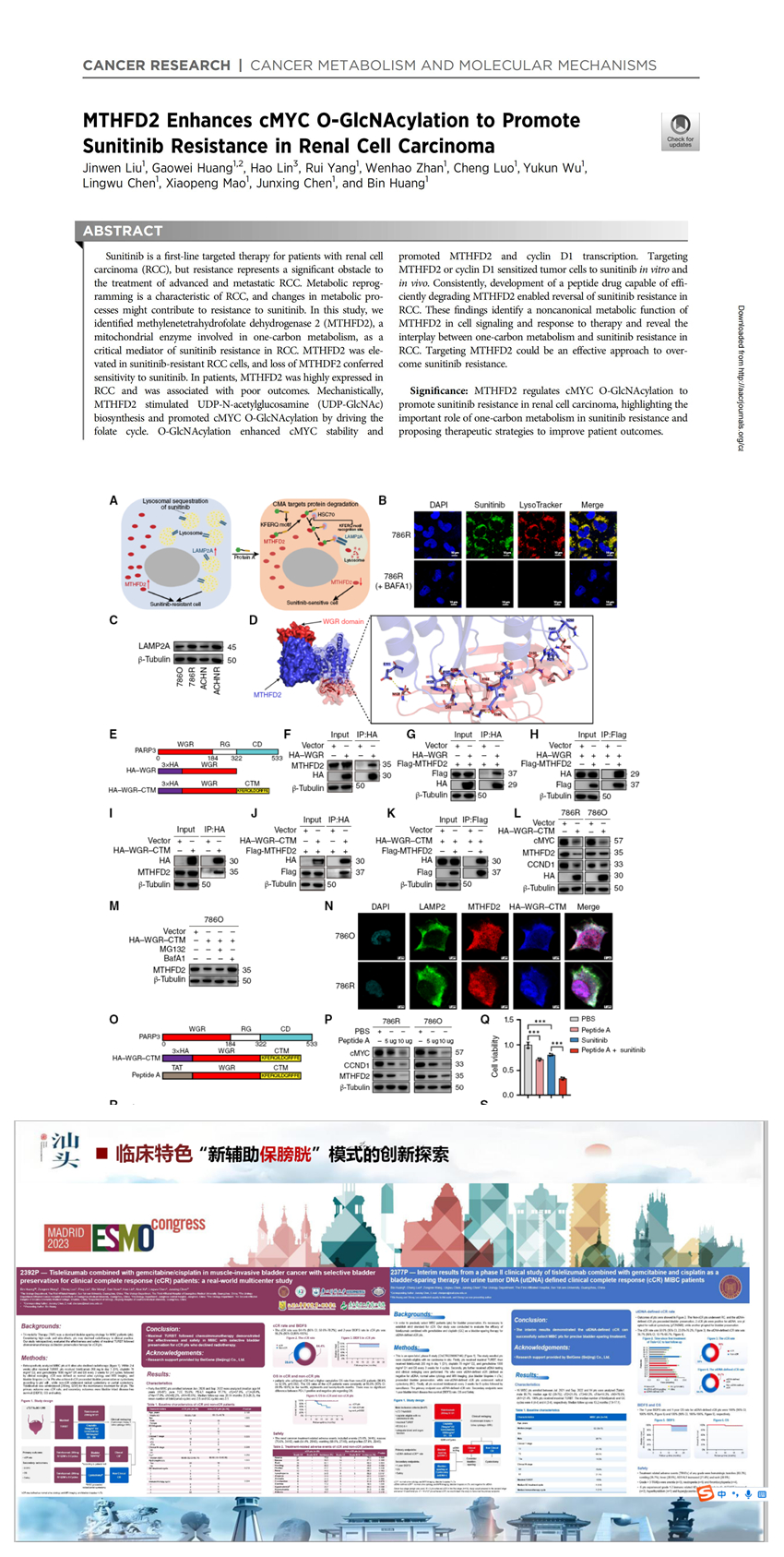
该论文研究了肾细胞癌靶向治疗的耐药机制,首次揭示了肾细胞癌中MTHFD2与O-GlcNAc糖基化修饰之间存在重要关联,MTHFD2能够通过其非经典酶功能影响葡萄糖摄取和AMPK/GFAT1信号轴,从而促进UDP-GlcNAc的生物合成,OGT介导的cMYC蛋白Thr58位点O-GlcNAc糖基化修饰可稳定cMYC蛋白,并增强其下游效应分子MTHFD2和CCND1的表达。这些研究发现不仅拓宽了我们对肾癌舒尼替尼耐药作用机制的认识,更揭示了靶向MTHFD2和CCND1联合分子伴侣介导的自噬(CMA)降解药物在肾癌治疗中的重要潜力。
突破性发现:MTHFD2可能是肾癌靶向耐药的关键“帮凶”
舒尼替尼是晚期肾癌的一线靶向药物,但耐药性严重制约其疗效。黄斌教授与林浩主任医师团队通过多组学分析,发现MTHFD2在耐药肿瘤细胞中异常高表达,且与患者不良预后显著相关。进一步研究发现,MTHFD2通过促进UDP-GlcNAc生物合成,增强致癌蛋白cMYC的O-GlcNAc修饰,形成“MTHFD2/O-GlcNAcylation/cMYC”正反馈环路,最终导致肿瘤细胞逃避舒尼替尼的杀伤作用。
尤为重要的是,团队成功开发出一种能特异性降解MTHFD2的肽类化合物“peptide A”在动物模型中证实其可显著恢复肿瘤细胞对舒尼替尼的敏感性。这一发现不仅阐明代谢酶调控耐药的非经典功能,更为临床克服肾癌靶向治疗耐药提供了可转化的干预靶点。
强强联合:院外兼聘教授制度结出科研硕果
黄斌教授作为中山大学附属第一医院泌尿外科杰出的青年专家,自受聘为汕头大学医学院第二附属医院泌尿外科兼聘教授以来,与附二院泌尿外科林浩主任医师团队在泌尿系统肿瘤精准治疗领域开展深度合作。在肌层浸润性膀胱癌保膀胱治疗领域,黄斌教授团队联合汕大医附二院泌尿外科林浩团队开展了三项临床研究,分别为免疫联合化疗回顾性保膀胱研究、免疫联合化疗前瞻性精准保膀胱研究以及免疫联合ADC前瞻性精准保膀胱研究,其中一项研究成果更是在2023年ESMO(欧洲肿瘤学年会)大会上以壁报形式展出。近年来,黄斌教授与林浩主任医师在泌尿外科本专业杂志上连续有高质量的论文发表。
通知类别:汕医新闻 撰稿人:附二院 审核人:组织宣传统战部
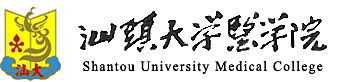






 最新要闻
最新要闻