我院药学系姜红岩和凌凯课题组在乳腺癌免疫治疗领域取得了重要进展。该团队携手第二附属医院甲乳外科李志扬主任和第一附属医院放射科黄瑞滨主任,通过药学、外科学和医学影像学的多学科交叉研究,共同研发出一种针对三阴性乳腺癌免疫治疗的新型纳米药物“BPNS@Mn²⁺/CpG”,研究成果"AMn2+/CpG Oligodeoxynucleotides Co-decorated Black Phosphorus Nanosheet Platform for Enhanced Antitumor Potency in Multimodal Therapy"近日在美国化学会旗舰期刊“ACS NANO”上发表,该期刊为自然指数期刊,影响因子为17.1。
肿瘤免疫疗法旨在激发人体自身免疫系统针对癌细胞的攻击并产生长效记忆,以减少肿瘤转移和复发,实现治愈。即便是如PD-1免疫检查点抑制剂和CAR-T细胞疗法等先进免疫治疗手段,要在复杂的实体瘤微环境中取得理想效果,也面临诸多挑战,这已成为当前肿瘤治疗领域研究的热点与挑战。
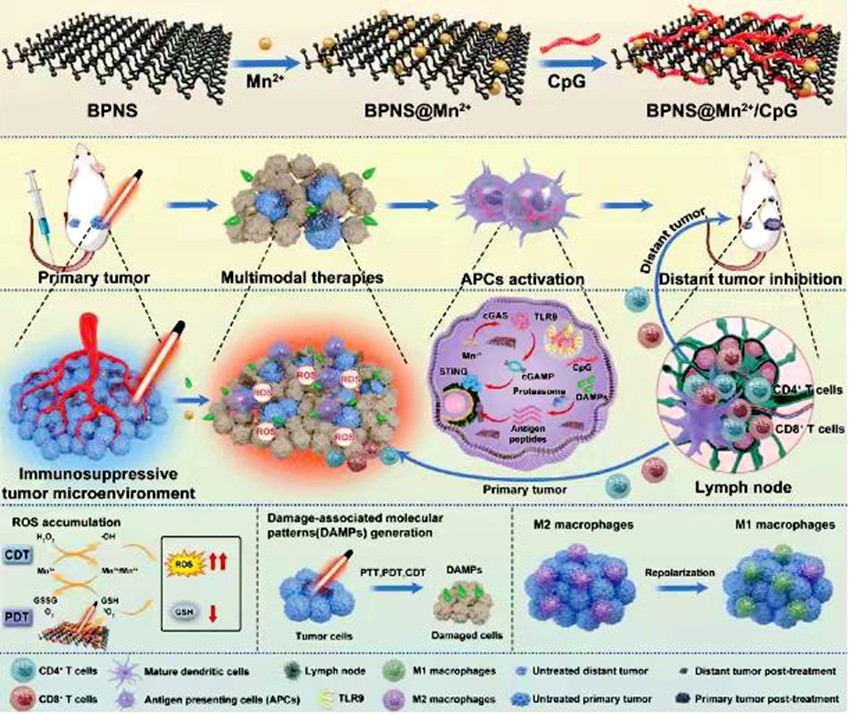
为了解决这一难题,该研究团队成功研发出新型纳米药物。该药物利用黑磷纳米片与锰离子(Mn²⁺)和CpG寡核苷酸进行复合,制备出“BPNS@Mn²⁺/CpG”纳米药物。在细胞及动物模型实验中,该药物表现出良好的稳定性,减少了非靶向的毒副作用。在乳腺癌的微酸性肿瘤环境中,该药物能够迅速分解并释放锰离子和CpG核酸药物,有效激活了肿瘤内的抗原递呈细胞,逆转了肿瘤微环境的免疫抑制状态。这一过程促使CD4+ 和 CD8+ T细胞汇聚至肿瘤部位对肿瘤细胞展开攻击,同时在淋巴结中扩充了记忆T细胞数量,从而激发出强烈的抗肿瘤免疫应答,阻止了乳腺癌的转移和术后复发。
由于该纳米药物结合了大量的锰离子,因此还可以用于体内肿瘤的实时磁共振成像(NMR),提高肿瘤治疗的靶向性,减少对健康组织的损伤。这一多模态治疗策略不仅改善了肿瘤微环境,还展现了在DNA/药物输送和肿瘤免疫治疗领域巨大的应用潜力。
BPNS@Mn²⁺/CpG纳米药物不仅实现了对乳腺癌肿瘤的多模态精准治疗,也成功调节了肿瘤微环境中的免疫抑制现象。该纳米药物高效的治疗效果,预示着其在DNA/药物传递及肿瘤免疫治疗领域应用的巨大潜力。这一研究成果由汕头大学医学院独立完成,展现了学院药学和乳腺癌免疫治疗领域的科研实力,更为其临床转化和应用研究奠定了坚实的基础,有望为乳腺癌治疗带来新的希望。
该纳米药物研发工作主要由医学院药学系完成,郑金涛、江晓红等药学系硕士研究生承担了该药物研发的具体工作,药学系黄乃琪教授提供了技术支持与帮助。研究团队负责人姜红岩副教授,硕士毕业于汕头大学医学院药理专业;后在北京协和医学院(清华大学医学部)获得医学博士学位,期间获得“北京市优秀毕业生”、“中国医学科学院优秀博士毕业论文”、“国家博士研究生奖学金”等多项荣誉。2017年由药学系主任石刚刚教授引进,回归母校药学系工作,已经在生物医学和药学领域取得了一系列成果,获得多项国家级和省部级课题项目,并在“Biosensors and Bioelectronics”等高水平期刊发表多篇研究论文,2022年获得“汕头市最美科技工作者”称号。


通知类别:汕医新闻 撰稿人:科研处 审核人:组织宣传统战部